 全球服务热线:400-086-8008
全球服务热线:400-086-8008- 日本语
 全球服务热线:400-086-8008
全球服务热线:400-086-8008

首页 > 医疗前沿资讯 > 海外前沿医讯 > 2015丙肝药物市场综评:复方制剂开创新局面
2015丙肝药物市场综评:复方制剂开创新局面
【本文为疾病百科知识,仅供阅读】 2015-08-12 作者:厚朴方舟
国外目前应用的丙肝治疗药物主要是聚乙二醇干扰素α-2a、特拉匹韦、波西普韦、索非布韦、利巴韦林等药物。据美国IMS数据,2013年全球七大市场500强畅销药中丙肝治疗药物市场规模为36亿美元,2014年有大幅度增长。2011年开始,国外丙肝治疗市场开始发力,到2014年达到高峰。近几年,美国FDA先后批准了6个丙肝治疗新药。
图1:
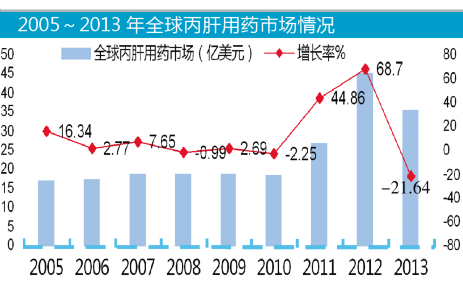
2011年5月13日,FDA批准了美国默沙东的丝氨酸蛋白酶抑制剂波普瑞韦(Boceprevir),商品名为Victrelis。波普瑞韦与聚乙二醇干扰素α、利巴韦林联合治疗丙肝。随后的2011年5月23日,FDA又批准了Vertex/强生制药公司研发的特拉瑞韦(Telaprevir),商品名为Incivek。特拉瑞韦是一种可逆的HCV NS3/4A蛋白酶抑制剂,能够直接攻击HCV,阻断其复制。特拉瑞韦与聚乙二醇干扰素α和利巴韦林联合治疗特定慢性丙肝。从已公布的Ⅲ期临床数据来看,特拉瑞韦与现行标准治疗药物合用,五年生存率可达79%。
据美国IMS数据,2013年,全球特拉匹韦市场规模为9.95亿美元,在索非布韦竞逐下,消费者转向了吉利德新药索非布韦,导致特拉瑞韦与聚乙二醇干扰素α和利巴韦林联合治疗用药市场的下滑。
图2:
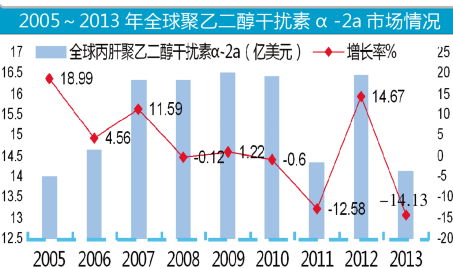
2013年11月22日,丙肝新药Simeprevir获得FDA批准,商品名为Olysio,在日本的商品名为Sovriad。联合聚乙二醇干扰素和利巴韦林用于基因1型慢性丙型肝炎成人患者代偿性肝脏疾病(包括肝硬化)的治疗。Simeprevir胶囊是新一代NS3/4A蛋白酶抑制剂,经FDA优先审评程序批准用于HCV GT1感染。
Olysio为每日一次的口服药物,由瑞典MedivirAB研发推出,随后被美国强生旗下的杨森公司收购,用于治疗慢性丙型肝炎成年患者的代偿性肝病,包括各个阶段的肝纤维化。这是第二代蛋白酶抑制剂,给药方式为:Simeprevir+聚乙二醇干扰素+利巴韦林联合治疗12周,随后进行聚乙二醇干扰素+利巴韦林治疗12周或36周。
Olysio与2011年上市的美国默沙东公司研发的丙型肝炎病毒蛋白酶抑制剂波普瑞韦(Boceprevir,Victrelis)以及2011年5月23日FDA批准Vertex制药公司的特拉匹韦(Telaprevir,Incivek)同样需要聚乙二醇干扰素+利巴韦林联合治疗。因此,在目前来看,这是第3个上市的NS3/4A蛋白酶抑制剂。这一类药只适用于HCV基因1型感染,而且需要与聚乙二醇干扰素、利巴韦林联用,同时也有不可预计的副作用。此外治疗也相当复杂,还有许多药物相互作用的潜在问题,而且对于其它基因型HCV感染患者尚未得到有效的作用,因此无法面对多方面挑战。在多个全口服丙肝药物上市的火红年代,重磅药物难逃昙花一现的结局。
从来没有过的索非布韦
目前,已经有近20种核苷酸和非核苷酸类NS5B抑制剂处于不同阶段的临床试验中。索非布韦是吉利德科学公司开发的核苷类NS5B聚合酶抑制剂,商品名为Sovaldi。FDA授予其“突破性药物资格”。2013年12月6日,美国FDA批准索非布韦用于基因1型、2型、3型和4型慢性丙型肝炎成人患者的治疗。在用于特定基因型2型和3型慢性丙型肝炎治疗时,可消除对传统注射药物干扰素的需求,单独口服索非布韦即可,不需与干扰素联用,因此是纯口服抗丙肝药物。但对于1型和4型HCV感染,仍需要与聚乙二醇干扰素、利巴韦林联用。
2011年,吉利德以110亿美元收购了总部位于美国新泽西州普林斯顿的丙肝治疗药生产商Pharmasset Inc,获得了正在研发的索非布韦等3种已进入临床阶段的慢性丙肝药物。索非布韦专利有效期至2029年3月26日。据国外媒体报道,索非布韦在美国的批发价格将为2.8万美元,即每片1000美元,大多数患者需要治疗12周,总费用将达8.4万美元。
图3:
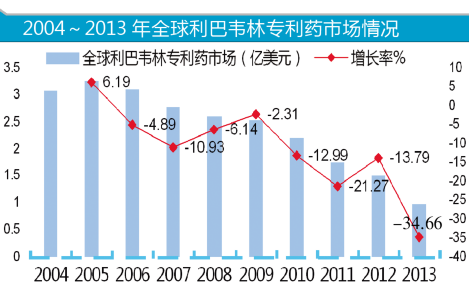
据美国IMS数据,2013年,全球索非布韦市场规模为1.40亿美元,分析师们预测索非布韦会成为一款超级重磅炸弹级产品。2014年,索非布韦销售额将达到19亿美元,2016年销售额将达到66亿美元。
复方开创新局面
2014年10月10日,FDA批准吉利德的索非布韦/雷迪帕韦复方制剂,商品名为Harvoni。这是前列个被批准治疗慢性HCV基因1型感染二联复方药物,也是前列个被批准不需要联用干扰素或利巴韦林的方案。
2014年12月19日,美国FDA批准了雅培生命-艾伯维公司的复方翁比他韦+帕利瑞韦+达萨布韦+利托那韦片联合包装,商品名为Viekira Pak。适应症为基因1型慢性丙型肝炎病毒感染,包括晚期肝硬化。这款组合产品名为Viekira Pak,它包含的3种新药Ombitasvir、Paritaprevir和Dasabuvir协同抑制HCV的增长。并包含此前获批的药物利托那韦,用于增加Paritaprevir的血液水平。3种新药属于蛋白酶抑制剂、NS5A抑制剂、非核苷聚合酶抑制剂,获得了突破性治疗方法资格认定。Viekira Pak是去年以来治疗慢性HCV感染第4个获批药品,可有或无利巴韦林联用,但对失代偿肝硬变者不建议使用。
随着人类科学的进步,我们正面对崭新靶点的挑战。不仅是对恶性肿瘤,对其它疾病也是如此,尤其是今天的新药研发已经和过去有所不同,崭新机理的出现,在机不逢时之际,今天风光无限,明日或许会是折戟沉沙。
厚朴方舟2012年进入海外医疗领域,总部位于北京,建立了由全球权威医学专家组成的美日名医集团,初个拥有日本政府官方颁发的海外医疗资格的企业。如果您有海外就医的需要,请拨打免费热线400-086-8008进行咨询!
本文由厚朴方舟编译,版权归厚朴方舟所有,转载或引用本网版权所有之内容须注明"转自厚朴方舟官网(www.hopenoah.com)"字样,对不遵守本声明或其他违法、恶意使用本网内容者,本网保留追究其法律责任的权利。
热门服务
推荐阅读
日本权威医学专家
日本医院排名
服务案例更多>
 全球咨询服务热线
全球咨询服务热线
400-086-8008

English | 微信端

互联网药品信息服务资格证书编号:(京)·非经营性·2015·0179
厚朴方舟健康管理(北京)有限公司 版权所有 www.hopenoah.com
京ICP备15061794号
京公网安备 11010502027115号