 全球服务热线:400-086-8008
全球服务热线:400-086-8008- 日本语
 全球服务热线:400-086-8008
全球服务热线:400-086-8008

首页 > 美国看病 > 美国新药资讯 > 美国看病-FDA批准 丙肝缓释剂新药
美国看病-FDA批准 丙肝缓释剂新药
【本文为疾病百科知识,仅供阅读】 2016-08-03 作者:厚朴方舟
出国看病服务机构厚朴方舟前沿消息,近日,生物制药公司艾伯维(AbbVie)宣布,美国FDA已经批准了其产品VIEKIRA XR缓释片的新药申请(NDA)。VIEKIRA XR是每日一次的缓释制剂,与先前获批产品VIEKIRA PAK一样,有效成分是dasabuvir、ombitasvir、paritaprevir和ritonavir,用于治疗基因1型的慢性丙型肝炎病毒成人感染者。他们包括伴有代偿性肝硬化的患者,但不包括那些晚期肝硬化伴有失代偿性肝硬化的丙肝患者。

▲获批产品VIEKIRA PAK
丙型肝炎是一种由于丙型肝炎病毒感染而引起的肝脏炎症疾病,它可导致肝功能下降、肝衰竭甚至肝癌。据美国CDC统计,大约有270万美国人感染有丙型肝炎病毒。根据世界卫生组织的数据,全球估计有1.7亿人患有慢性丙型肝炎,每年有大约有50万人死于与丙肝相关的肝脏疾病。大多数感染有丙型肝炎病毒的人在肝脏损伤变得明显之前没有疾病症状,如果不进行正常治疗,这一感染过程在20到30年后,其中有10-20%的患者个体会发展为肝硬化和肝癌。目前,尚无预防丙型肝炎病毒感染的疫苗。
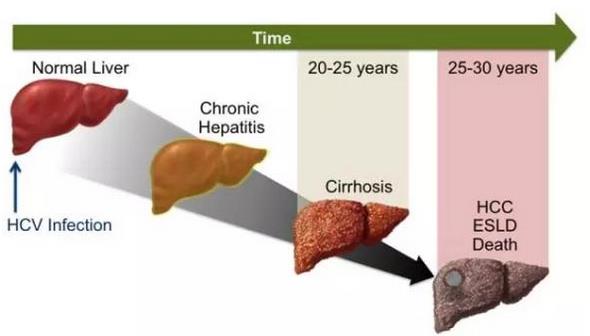
▲感染丙肝病毒后恶化过程
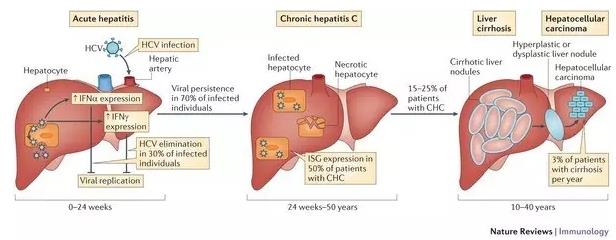
▲丙肝病毒在体内的繁殖过程
丙肝病毒有六种不同的基因型,不同的基因型对药物反应也不同。其中1型是较常见的丙肝亚型,约占60%。以往丙肝的治疗方法以干扰素和利巴韦林(Ribavirin)为基础,需要每周静脉注射,经48周疗程后,五年生存率仍只有50%左右。
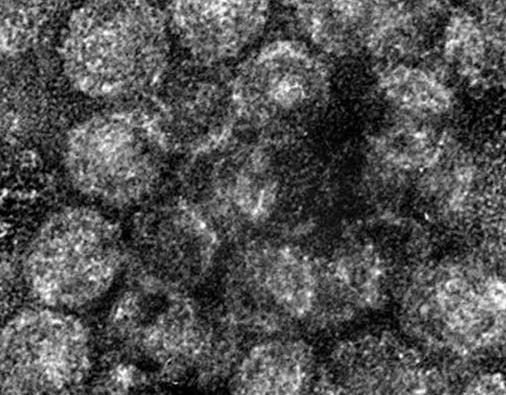
▲电镜下的丙肝病毒颗粒
VIEKIRA XR是一个由200毫克dasabuvir、8.33毫克ombitasvir、50毫克paritaprevir和33.33毫克ritonavir组合的缓释片剂,每日一次给药三粒,必须与食物一起服用。
FDA对VIEKIRA XR的批准是基于七个3期临床试验的良好数据,2300多名患者接受VIEKIRA PAK治疗后有非常高的五年生存率。同时,VIEKIRA XR也通过了与VIEKIRA PAK比较的两项生物制剂等效性试验。
艾伯维的副总裁兼首席医疗官Rob Scott博士说道:“艾伯维致力于继续推动丙型肝炎的治疗护理,这是我们对患者持续承诺的积极表现。VIEKIRA XR的成分被临床试验数据证明针对基因1b型患者有满分的五年生存率,VIEKIRA XR的新药申请获批为1型丙肝患者提供了新的治疗选择方案。”
厚朴方舟2012年进入海外医疗领域,总部位于北京,建立了由全球权威医学专家组成的美日名医集团,初个拥有日本政府官方颁发的海外医疗资格的企业。如果您有海外就医的需要,请拨打免费热线400-086-8008进行咨询!
本文由厚朴方舟编译,版权归厚朴方舟所有,转载或引用本网版权所有之内容须注明"转自厚朴方舟官网(www.hopenoah.com)"字样,对不遵守本声明或其他违法、恶意使用本网内容者,本网保留追究其法律责任的权利。
上一篇:美国医疗-乳腺癌新药3期临床效果显著,已向FDA提交新药申请 下一篇:美国看病-淋巴瘤上市药物新3期临床试验结果良好
热门服务
推荐阅读
美国权威医学专家
美国医院排名
 全球咨询服务热线
全球咨询服务热线
400-086-8008

English | 微信端

互联网药品信息服务资格证书编号:(京)·非经营性·2015·0179
厚朴方舟健康管理(北京)有限公司 版权所有 www.hopenoah.com
京ICP备15061794号
京公网安备 11010502027115号