 全球服务热线:400-086-8008
全球服务热线:400-086-8008- 日本语
 全球服务热线:400-086-8008
全球服务热线:400-086-8008
美国看病
低级别胶质瘤一般指WHO1~2级的胶质瘤,肿瘤生长缓慢,是儿童常见的原发性脑恶性肿瘤之一。虽然低级别胶质瘤恶性程度较低,但是由于低级别胶质瘤很难完全切除,且复发率较高,多次复发后可能进展为胶质瘤,因此需要有效的药物来提高预后效果。
[美国新药资讯]2024/04/26
双靶治疗肺癌BRAF V600E突变美国获批-Braftovi联合Mektovi缓解率达75%
10月12日,美国FDA批准Braftovi(encorafenib)与Mektovi(binimetinib)组合治疗的补充新药申请(sNDA),用以治疗经FDA核准测试带有BRAF V600E突变的转移性非小细胞肺癌(NSCLC)患者。
[美国新药资讯]2023/10/16
国外新治疗卵巢癌的药物有哪些?美国日本治疗卵巢癌五年生存率高,日本治疗卵巢癌的平均5年生存率为64.5%;美国治疗卵巢癌的平均5年生存率为50%;国内卵巢癌的平均5年生存率为39.1%。美国日本的高生存率优势,除了更好的设备、精细的手术技巧等外,与更多的新药选择、更规范的药物治疗方案也有很大关系。本文将对美国日本卵巢癌新药进行介绍。
[美国新药资讯]2023/09/05
[美国新药资讯]2023/09/04
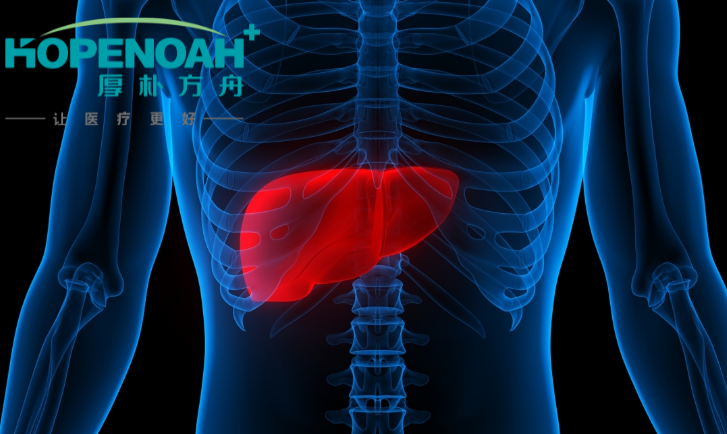
日本美国免疫联合治疗肝癌晚期效果如何?近年来,随着免疫抑制剂的出现,晚期肝癌治疗的选择不断增多,生存期也在稳步增长。本文将对国际治疗肝癌晚期的免疫联合方案及效果进行介绍。

美国前列腺新药Akeega获批-用于BRCA阳性转移性去势抵抗性前列腺癌患者
[美国新药资讯]2023/08/15
近日,美国FDA批准Akeega(PARP抑制剂Zejula和醋酸阿比特龙构成的双效片剂)与强的松(prednisone)一起给药,用于治疗经美国FDA批准检测证实带有BRCA基因突变阳性的转移性去势抵抗性前列腺癌(mCRPC)成人患者。Akeega成为率先获批的,结合PARP抑制剂与醋酸阿比特龙、具双重机制的口服片剂。该前列腺癌新药效果如何?(想要预约美国权威医院看病或全程会诊的前列腺癌患者可以拨打免费热线400-086-8008进行咨询)
[美国新药资讯]2023/07/07
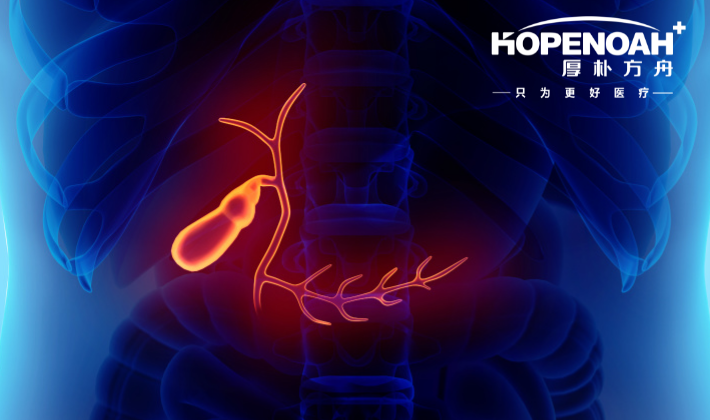
美国有治疗胆管癌的靶向药吗?胆管癌治疗难度较大,多数患者确诊时已经是晚期,美国的新药和新临床试验更多,可以为患者带来更多治疗选择,为许多国内现有治疗方案束手无策的胆管癌患者带来了新希望。那么国外有哪些治疗胆管癌的新药?
帕博利珠单抗-Larotrectinib...这5款广谱抗癌药物效果如何
[美国新药资讯]2023/04/11
全球已有5款“不限癌种”广谱抗癌药物获批上市。帕博利珠单抗pembrolizumab、Larotrectinib (Vitrakvi)、Entrectinib(Rozlytrek)、Tafinlar+Mekinist组合方案、Retevmo(selpercatinib),这些方案治疗癌症效果如何?

[美国新药资讯]2023/02/23
近日PARP抑制剂Talzenna(talazoparib)与Xtandi(恩扎卢胺,enzalutamide)构成的组合治疗用于转移性去势抵抗性前列腺癌(mCRPC)患者(无论是否带有同源重组修复(HRR)基因突变)的补充新药申请已获得美国FDA授予的优先审评资格。

美国新药丨首款HER2阳性结直肠癌组合疗法获美国FDA加速批准
[美国新药资讯]2023/01/29
对于标准治疗失败的HER2扩增或过表达的晚期结直肠癌患者,靶向HER2的治疗可延长患者的生存期。1月19日,美国FDA加速批准其HER2抑制剂Tukysa(tucatinib),与HER2单克隆抗体Trastuzumab联用,治疗接受化疗后疾病出现进展的RAS野生型、HER2阳性无法切除或转移性结直肠癌患者,这是FDA批准的初款针对HER2阳性结直肠癌的方案。
[美国新药资讯]2023/01/04
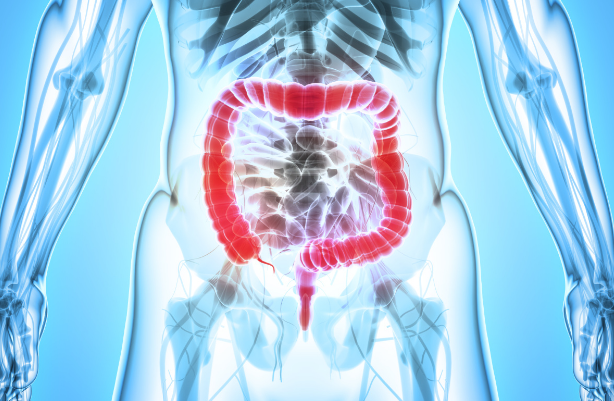
根据调查数据显示约50%-60%的结直肠癌患者会出现肝脏转移,近20%-30%的患者确诊时已经出现了肝脏转移。但是随着医疗技术的不断进步,越来越多的结直肠癌肝转移患者在合理治疗后获得了良好的预后。那么,针对结直肠癌肝转移,美国常用的治疗手段有哪些?
美国权威医学专家
美国医院排名
 全球咨询服务热线
全球咨询服务热线
400-086-8008

English | 微信端

互联网药品信息服务资格证书编号:(京)·非经营性·2015·0179
厚朴方舟健康管理(北京)有限公司 版权所有 www.hopenoah.com
京ICP备15061794号
京公网安备 11010502027115号